Что заставляет жизнь тикать? Митохондрии могут сохранять время для клеток
Что заставляет жизнь тикать? Митохондрии могут сохранять время для клеток

Каждый вид развивается в своем уникальном темпе, и ученые задаются вопросом, что управляет этим временем. Ряд новых результатов предполагает, что клетки используют основные метаболические процессы как часы.
Точно так же, как люди в разных местах действуют в разных ритмах, то же самое происходит и с разными биологическими видами. Они стареют со своей собственной скоростью: некоторые, например плодовая мушка, стремятся к взрослой жизни, чтобы иметь возможность размножаться до того, как исчезнет их эфемерный источник пищи, в то время как такие существа, как люди, взрослеют медленно, в течение десятилетий, отчасти потому, что этого требует построение большого и сложного мозга. А в самом начале жизни эмбриона небольшие изменения во времени и способе развития различных тканей могут радикально изменить форму организма — механизм, который эволюция использует при создании новых видов. Однако что задает темп роста организма, так и осталось загадкой.
«Наши знания о том, что контролирует сроки развития, действительно отстают от других областей биологии развития», — сказала Маргарет Диас Куадрос, которая возглавляет исследования, посвященные темпам развития, в Массачусетской больнице общего профиля в Бостоне.
Биологи развития добились огромных успехов в выявлении сетей регуляторных генов, которые взаимодействуют друг с другом — каскадных систем петель обратной связи, которые включают или выключают гены точно в нужное время и в нужном месте для построения, скажем, глаза или ноги. Но высококонсервативное сходство этих генных сетей среди видов контрастирует с огромными различиями во времени развития. Мыши и люди, например, используют одни и те же наборы генов для создания нейронов и позвоночника. Однако мозг и позвоночник мыши устроены совсем иначе, чем у человека, потому что время активности этих генов различно, и неясно, почему это так.
«Генная регуляция, похоже, не объясняет всего, что касается сроков развития», — сказал Пьер Вандерхаэген, изучающий эволюцию и развитие мозга в Левенском университете в Бельгии. «Это немного провокационно, потому что в биологии все должно быть объяснено регуляцией генов, прямо или косвенно».

Маргарет Диас Куадрос и ее коллеги из Гарвардской медицинской школы создали модель часов сегментации, которые моделируют позвоночник позвоночных, в стволовых клетках мыши и человека.
Новые объяснения того, что заставляет жизнь жить, появляются благодаря инновациям — таким как достижения в области культуры стволовых клеток и доступности инструментов для управления метаболизмом, первоначально разработанных для изучения рака — которые теперь позволяют исследователям составлять графики и экспериментировать с темпами развития ранних видов рака. эмбрионы и ткани более подробно. В ряде работ за последние несколько лет, включая одну ключевую публикацию в июне, несколько исследовательских групп независимо друг от друга пришли к выводу об интригующих связях между темпом развития, скоростью биохимических реакций и скоростью экспрессии генов, лежащих в основе этих биохимических реакций.
Их результаты указывают на общий метроном: митохондрии, которые могут быть хранителями времени клетки, задавая ритм для различных процессов развития и биохимических процессов, которые создают и поддерживают жизнь.
Нейрон сохраняет время
Более десяти лет назад Вандерхаген провел эксперимент, который заложил основу для современных исследований о том, как поддерживается темп развития. Нейробиолог находился в своей бельгийской лаборатории, выращивая стволовые клетки в чашках Петри и наблюдая, как долго они созревают от пустых клеточных досок до полноценных нейронов, соединяющихся и взаимодействующих с другими. Он думал, что сможет найти ключ к разгадке происхождения и эволюции человеческого мозга, сравнив стволовые клетки мыши и человека, готовые стать нейронами.
Первое, что он заметил, это то, что стволовые клетки мыши дифференцируются в зрелые клетки мозга примерно за неделю — быстрее, чем стволовые клетки человека, рост которых занимает от трех до четырех месяцев.

Более десяти лет назад нейробиолог Пьер Вандерхаген (слева) из Левенского университета в Бельгии обнаружил, что темп развития присущ самой клетке. Совсем недавно он и Рёхей Ивата (справа) изучали, могут ли митохондрии быть движущей силой этого процесса.
С разрешения Пьера Вандерхагена (слева); С разрешения Рёхея Иваты
Но будут ли эти клетки развиваться таким же образом в растущем мозге, а не в изолированной чашке? Чтобы выяснить это, он пересадил нейрон мыши в мозг живой мыши. Клетка следовала той же временной шкале, что и нейроны мыши-хозяина, дифференцируясь примерно через неделю. Затем он попробовал то же самое с человеческим нейроном, имплантировав его в мозг мыши. К его изумлению, человеческий нейрон сохранял собственное время. Несмотря на то, что он находился в среде обитания грызунов, на его созревание ушёл почти год.
«Это дало нам первый важный ответ: каким бы ни был механизм синхронизации, большая часть его, по-видимому, находится в самих нейронах», — сказал Вандерхэген. «Даже если вы вытащите клетки из чашки Петри и поместите их в другой организм, они все равно сохранят свою собственную временную шкалу».
Тем не менее, еще пару лет назад практически ничего не было известно об основном клеточном механизме.
Вандерхэген начал думать о том, откуда берутся строительные блоки нейрона. «Создавать нейроны — это все равно, что строить сверхсложное здание», — сказал он. «Вам нужна хорошая логистика». Клеткам нужна не только энергия, но и источник сырья для роста и деления.
Он подозревал, что митохондрии могут служить источником этих строительных блоков. Органеллы играют ключевую роль в росте и метаболизме клетки. Они производят энергию, за что их прозвали «электростанцией клетки», а также производят метаболиты, необходимые для построения аминокислот и нуклеотидов, а также для регулирования экспрессии генов.
Классический взгляд на митохондрии заключается в том, что они не меняются в течение жизни клетки. «Они просто милые, живописные маленькие сосиски в клетке, и они дают энергию», — сказал Вандерхэген. Но когда он и Рёхей Ивата, научный сотрудник его лаборатории, более внимательно изучили развитие нейронов, они увидели, что митохондриям тоже нужно время для развития.
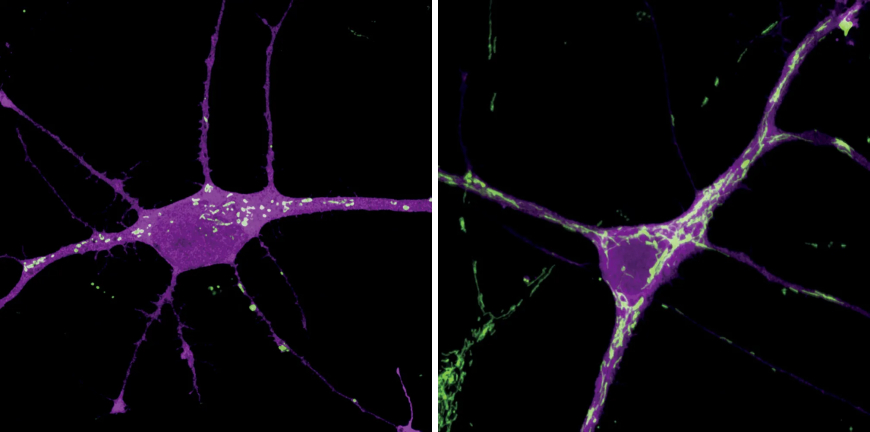
Митохондрии (окрашены в зеленый цвет) не являются статичными на протяжении всей жизни клетки. По мере взросления молодого нейрона (слева) органеллы растут в количестве, генерируют больше энергии и принимают характерную форму бобов (справа).
В молодых нейронах, как они сообщили в Science, было мало митохондрий, а те, что у них были, были фрагментированы и производили мало энергии. Затем, по мере взросления нейронов, количество, размер и метаболическая активность митохондрий росли. Более того, изменения происходили быстрее у мышей, чем у людей. По сути, система масштабировалась: созревание митохондрий синхронизировалось с созреванием нейронов у обоих видов.
Это открытие показалось Вандерхегену и Ивате важным. И это заставило их задуматься, могут ли митохондрии быть тихим барабанным боем, вызывающим огромные различия в темпах развития между видами.
Как вырастить позвоночник
Одной из классических моделей изучения темпа эмбрионального развития является формирование рисунка позвоночника. У всех позвоночных есть позвоночник, состоящий из цепочки позвоночных сегментов, но виды различаются по их количеству и размеру. Поэтому возникает естественный вопрос о механизмах развития, которые приводят к возникновению этой важной особенности позвоночных и ее многочисленных вариаций в животном мире.
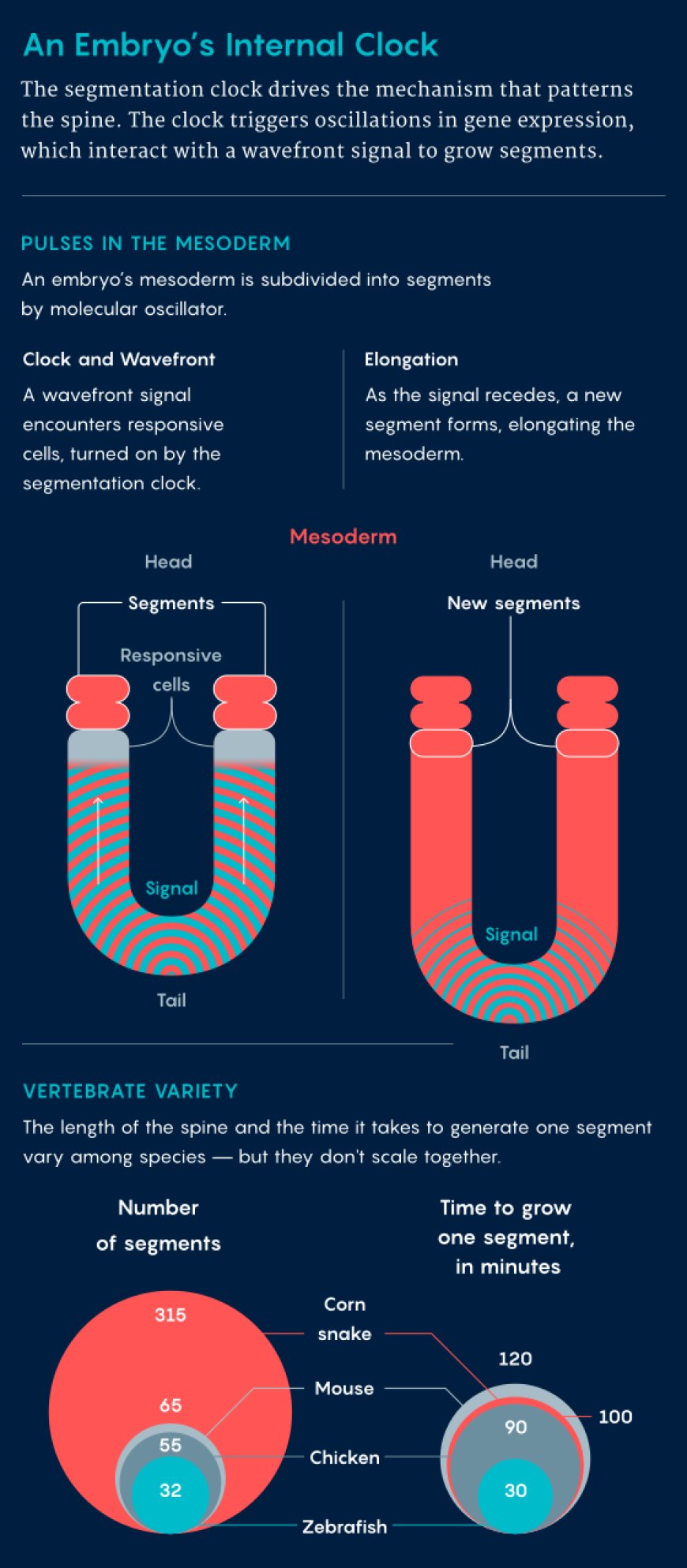
В 1997 году биолог развития Оливье Пурке, сейчас работающий в Гарвардской медицинской школе, впервые обнаружил молекулярный осциллятор, называемый часами сегментации, который управляет механизмом, формирующим структуру позвоночника позвоночных. Работая с куриными эмбрионами, его исследовательская группа определила ключевых игроков, которые ритмично экспрессируются во время формирования каждого сегмента позвонка в эмбриональной ткани. Часы сегментации запускают колебания экспрессии генов, заставляя клетки колебаться в своей реакции на сигнал волнового фронта, который движется от головы к хвосту. Когда волновой фронт встречает реагирующие клетки, формируется сегмент. Таким образом, механизм часов и волнового фронта управляет периодической организацией позвоночника.

По мнению Оливье Пурке из Гарвардской медицинской школы, исследования показывают, что существует «глобальная команда», которая управляет всеми процессами синхронизации развития.
Гены, управляющие часами сегментации, консервативны у разных видов. Однако период тактов — время между двумя пиками колебаний — не таков. В течение многих лет генетики развития не могли объяснить это: у них не было генетических инструментов, позволяющих точно манипулировать часами растущего эмбриона. Итак, примерно в 2008 году Пурке начал разрабатывать методы, позволяющие лучше анализировать механизм в лаборатории.
В то время «это звучало как настоящая научная фантастика», сказал он. Но эта идея стала более правдоподобной в течение следующего десятилетия, когда лаборатория Пурке и другие лаборатории по всему миру научились культивировать эмбриональные стволовые клетки и даже создавать органоиды — такие как сетчатка, кишечник или мини-мозг — в чашке.
Пурке и Диас Куадрос, тогда его аспирант, нашли способ воспроизвести часы в стволовых клетках мыши и человека. В ранних экспериментах они заметили, что период тактового сигнала у мышей составляет около двух часов, тогда как в клетках человека для завершения колебания требуется около пяти часов. Это был первый случай, когда кто-либо определил тактовый период сегментации у людей.
Другие лаборатории также увидели потенциал этих достижений в области биологии стволовых клеток для решения давних вопросов о сроках развития. В 2020 году две исследовательские группы — одну под руководством Мики Эбисуи из Европейской лаборатории молекулярной биологии в Барселоне, а другую под руководством Джеймса Бриско из Института Фрэнсиса Крика в Лондоне — независимо друг от друга обнаружили, что основные молекулярные процессы в клетке идут в ногу со скоростью эволюции. разработка. Они в журнале Science опубликовали исследования .
Команда Эбисуи хотела понять различия в скорости молекулярных реакций — экспрессии генов и деградации белков — которые управляют каждым тактовым циклом. Они обнаружили, что оба процесса в клетках мыши работают в два раза быстрее, чем в клетках человека.
Вместо этого Бриско рассмотрел раннее развитие спинного мозга. Как и тактовый цикл сегментации, процесс дифференцировки нейронов, включая экспрессию последовательностей генов и распад белков, у людей был пропорционально растянут по сравнению с мышами. «Чтобы достичь той же стадии развития с использованием эмбриональных стволовых клеток человека, требуется в два-три раза больше времени», — сказал Бриско.
Как будто внутри каждой клетки тикал метроном. С каждым колебанием маятника различные клеточные процессы — экспрессия генов, деградация белков, дифференцировка клеток и эмбриональное развитие — шли в ногу со временем.
Но было ли это общим правилом для всех позвоночных, за исключением мышей и людей? Чтобы выяснить это, аспирант Эбисуи Хорхе Ласаро создал «зоопарк стволовых клеток», в котором обитают клетки различных млекопитающих: мышей, кроликов, крупного рогатого скота, носорогов, людей и мартышек. Когда он воспроизвел часы сегментации каждого вида, он увидел, что скорость биохимических реакций у каждого вида оставалась в ритме с периодом часов сегментации.
Более того, темп часов не соответствовал размеру животных. Клетки мыши колебались быстрее, чем клетки носорога, но человеческие клетки колебались медленнее, чем клетки носорога, а клетки мартышек имели самые медленные колебания из всех.
Результаты, опубликованные в журнале Cell Stem Cell в июне, позволяют предположить, что скорость биохимических реакций может быть универсальным механизмом регулирования времени развития.
Они также раздвинули границы важного, но упускаемого из виду аспекта центральной догмы молекулярной биологии. «Мы говорим о транскрипции, трансляции и стабильности белков», — сказал Диас-Куадрос. Все думали, что они одинаковы у всех видов млекопитающих и позвоночных, «но теперь мы говорим, что скорость центральной догмы видоспецифична, и я думаю, что это весьма увлекательно».
Создать или уничтожить белок
Таким образом, часы должны быть основаны на механизме, который задает темп биохимических реакций у разных видов. Тереза Район хотела раскрыть его происхождение, когда наблюдала за дифференцировкой мотонейронов в своей лондонской лаборатории, где она училась под руководством Бриско.
Она генетически спроектировала развивающиеся нейроны мыши и человека, чтобы они экспрессировали флуоресцентный белок, который ярко светится при воздействии лазера на нужной длине волны. Затем она наблюдала за тем, как введенные белки разлагаются. К ее удивлению, одни и те же флуоресцентные белки в клетках мыши распадались быстрее, чем в клетках человека, идя в ногу с развитием нейронов. Это навело ее на мысль, что что-то во внутриклеточной среде задает темп деградации.

Наблюдая за тем, как белки деградируют с постоянной скоростью в развивающихся нейронах, Тереза Район, сейчас работающая в Институте Бабрахама в Англии, начала искать механизм, который задает темп метаболизма.
«Если бы вы спросили биолога: «Как определить стабильность белка?» они скажут вам, что все зависит от последовательности», — сказала Район, которая сейчас возглавляет собственную лабораторию в Институте Бабрахама в Кембридже, Англия. «Однако мы обнаружили, что на самом деле это не так. Мы думаем, что свою роль может сыграть механизм, разрушающий белки».
Но она и ее группа изучали только один тип клеток. Если типы клеток в разных тканях развиваются с разной скоростью, будут ли их белки деградировать с разной скоростью?
Майкл Доррити из Европейской лаборатории молекулярной биологии в Гейдельберге изучал этот вопрос, размышляя о том, как температура влияет на развитие. Многие животные, от насекомых до рыб, развиваются быстрее, если их выращивать при более высоких температурах. Интересно, что он заметил, что у эмбрионов рыбок данио, выращенных в теплой среде, темп развития некоторых типов клеток ускорялся быстрее, чем других.
В препринте, который он опубликовал в прошлом году, он остановился на объяснении механизмов, которые производят и расщепляют белки. Некоторым типам клеток требуется больший объем или более сложные белки, чем другим. В результате некоторые типы клеток хронически «нагружают механизмы контроля качества белка», сказал он. Когда температура повышается, они не могут удовлетворить более высокие потребности в белке, и поэтому их внутренние часы не могут ускориться и идти в ногу со временем.
В этом смысле организмы не имеют единых унифицированных часов, а имеют множество часов для многих тканей и типов клеток. С эволюционной точки зрения это не ошибка, а особенность: когда ткани развиваются не синхронно друг с другом, части тела могут расти с разной скоростью, что может привести к эволюции разнообразных организмов или даже новых видов.

Майкл Доррити смотрит на синий аквариум с маленькими плавающими рыбками в комнате, уставленной такими же аквариумами.
Майкл Доррити из Европейской лаборатории молекулярной биологии в Гейдельберге обнаружил, что каждая ткань эмбрионов рыб данио имеет свои собственные часы развития, которые определяют, насколько быстро созревает тип клеток.
До сих пор эти механизмы во всех системах и масштабах — в часах сегментации развивающегося эмбриона, в отдельном развивающемся нейроне и в более фундаментальных белковых механизмах — все продолжали работать вовремя.
«Практически все, что мы до сих пор рассматривали, является масштабированием, — сказал Пурке, — а это означает, что для всех этих процессов существует глобальное управление».
Тик-так метаболизма
Какой может быть эта система управления выше по потоку? Пурке и Диас Куадрос задумались над тем, какая система потенциально может влиять на различные клеточные процессы, и остановились на метаболизме, управляемом митохондриями. Митохондрии производят АТФ, энергетическую валюту клетки, а также множество метаболитов, необходимых для построения белков и ДНК, регулирования генома и выполнения других важных процессов.
Где-то в их геноме должна быть разница в последовательностях между мышью и человеком, которая кодирует эту разницу в скорости развития.
Маргарет Диас Куадрос, Массачусетская больница общего профиля
Чтобы проверить эту идею, они разработали генетические и фармакологические методы, позволяющие ускорить, а затем замедлить скорость метаболизма стволовых клеток. Если митохондрии действительно задавали клеточный темп, они ожидали, что их эксперименты изменят ритм часов сегментации.
Когда они замедлили метаболизм в клетках человека, часы сегментации тоже замедлились: их период увеличился с пяти до семи часов, а также замедлилась скорость синтеза белка. А когда они ускоряли обмен веществ, колебания часов тоже ускорялись.
Они словно открыли ручку настройки внутреннего метронома клетки, позволяющую ускорять или замедлять темп эмбрионального развития. «Эти различия во времени объясняются не различиями в архитектуре регуляции генов», — сказал Пурке. Результаты были опубликованы в журнале Nature ранее в этом году.
Эта ручка метаболической настройки не ограничивалась развивающимся эмбрионом. Тем временем Ивата и Вандерхэген придумали, как использовать лекарства и генетику, чтобы играть с метаболическим темпом созревающих нейронов — процесс, который, в отличие от часов сегментации, которые работают всего пару дней, занимает много недель или месяцев. Когда нейроны мыши были вынуждены генерировать энергию медленнее, нейроны также созревали медленнее. И наоборот, фармакологически сдвигая человеческие нейроны в сторону более быстрого пути, исследователи могли ускорить их созревание. Результаты были опубликованы в журнале Science в январе.
Для Вандерхегена вывод их экспериментов ясен: «Скорость метаболизма определяет сроки развития».
Тем не менее, даже если метаболизм является вышестоящим регулятором всех других клеточных процессов, эти различия должны сводиться к генетической регуляции. Вполне возможно, что митохондрии влияют на время экспрессии генов развития или тех, кто участвует в механизме создания, поддержания и переработки белков.
Одна из возможностей, предположил Вандерхэген, заключается в том, что метаболиты митохондрий необходимы для процесса конденсации или расширения свернутой ДНК в геномах, чтобы ее можно было транскрибировать для построения белков. Возможно, предположил он, эти метаболиты ограничивают скорость транскрипции и глобально определяют скорость включения и выключения генных регуляторных сетей. Однако это всего лишь одна идея, которая нуждается в экспериментальном раскрытии.
Существует также вопрос о том, что вообще заставляет митохондрии работать. Диас Куадрос считает, что ответ должен лежать в ДНК: «Где-то в их геноме должна быть разница в последовательностях между мышью и человеком, которая кодирует эту разницу в скорости развития».
«Мы до сих пор понятия не имеем, в чем заключается эта разница», — сказала она. «К сожалению, мы еще очень далеки от этого».
Поиск этого ответа может занять время, и, как и митохондриальные часы, научный прогресс идет в своем собственном темпе.
Исправление: 18 сентября 2023 г.
Во введении предложение было изменено, чтобы уточнить, что именно скорость экспрессии генов, а не общая скорость метаболизма, помогает управлять темпом развития. Статья также была обновлена, чтобы уточнить, какие виды в зоопарке стволовых клеток имеют самые быстрые и самые медленные колебания часов сегментации.
Какова ваша реакция?










































































![Ко всему трудовому крестьянству. О съезде Всероссийского крестьянского союза [листовка]. — Петроград, 1917](https://uzmedlib.uz/uploads/images/202604/image_430x256_69d4e443a1936.jpg)